はじめに
バイオテクノロジーとデジタル技術の融合が加速する現代において、新たな研究分野「デジタルバイオロジー」が急速に発展しています。特に2025年に入り、AIと生物学の統合がもたらす可能性に大きな注目が集まっています。従来の生物学研究は長い実験時間と膨大なリソースを必要としましたが、AI基盤モデルの登場により研究プロセスが劇的に変化しつつあります。
本記事では、デジタルバイオロジーとAI基盤モデルの最新動向について掘り下げ、この革新的な技術が医療や創薬、そして私たちの生活にどのような影響をもたらすのかを探っていきます。
デジタルバイオロジーとは何か?
デジタルバイオロジーとは、生物学(バイオロジー)と情報科学(インフォマティクス)を融合させた学問分野です。生物学的データをデジタル解析することで、生命現象の理解を深め、医療や農業、環境科学などの幅広い分野に革新をもたらします。
ゲノム解析から始まったこの分野は、現在では以下のような領域に発展しています:
- 生体分子の構造・機能予測:タンパク質の折りたたみや機能を予測
- システム生物学:生物学的ネットワークをモデル化し理解
- 個別化医療:個人のゲノム情報に基づいた治療法の設計
- 創薬研究:新薬候補の探索と開発プロセスの加速
従来の「試行錯誤」に基づく実験的アプローチから、「予測と検証」に基づくデータ駆動型アプローチへと生命科学研究のパラダイムが変化しているのです。
2025年注目のAI基盤モデル技術
2025年に入り、バイオテクノロジー分野でのAI基盤モデルの開発が急速に進んでいます。AI基盤モデルとは、大規模なデータセットで事前学習され、様々なタスクに適応可能な汎用的なAIモデルを指します。
バイオ基盤モデルの特徴
韓国科学技術情報通信部(MSIT)と韓国生命工学研究院(KRIBB)が発表した「2025年10大有望バイオテクノロジー」の中でも、「バイオ基盤モデル」が注目技術の一つとして選出されました。バイオ基盤モデルには以下のような特徴があります:
- マルチモーダル学習:ゲノム、タンパク質構造、細胞画像など多様なデータタイプを統合的に処理
- ゼロショット能力:未知の生物学的問題に対しても一定の推論能力を発揮
- 知識転移:複数の生物学的タスク間で知識を転用可能
- スケール効果:データと計算リソースを増やすことで性能が向上
先進企業の動向
2025年現在、複数のスタートアップ企業やテック企業がバイオ基盤モデルの開発に取り組んでいます:
- Latent Labs:DeepMindのAlphaFold2の上級科学研究員であったSimon Kohl博士によって設立。2025年2月に総額5,000万ドルの資金を調達し、生物学をプログラム可能にするためのAI基盤モデルを構築中。
- Bioptimus:生物学に特化したAI基盤モデルを開発するフランスのスタートアップで、3,500万ドルの資金を調達。
- NVIDIA:デジタル・バイオロジー部門が開発したEVO 2という原核生物から全生物界に対応したAIモデルを発表。機能不明だった遺伝子の機能推測や新機能を持つゲノム生成が可能。
これらの企業は、AIが生物学研究の効率とスピードを向上させる可能性に注目し、積極的に投資を行っています。
デジタルバイオロジーがもたらす医療革命
デジタルバイオロジーとAI基盤モデルの進化は、医療分野に革命的な変化をもたらす可能性を秘めています。
個別化医療の実現
従来の医療では「一般的な患者」を対象とした治療法が主流でしたが、デジタルバイオロジーとAI基盤モデルの発展により、個人の遺伝情報や環境要因を考慮した真の個別化医療が実現しつつあります:
- 遺伝子変異の影響予測:個人の遺伝子変異がどのような疾患リスクをもたらすかをAIが高精度に予測
- 最適薬剤の選定:薬物代謝に関わる遺伝的多型に基づいた最適な薬剤選択
- 治療反応性の予測:治療への反応性を事前に予測し、無駄な治療を回避
創薬プロセスの変革
新薬開発には通常10年以上の時間と数千億円のコストがかかりますが、AI基盤モデルを活用することで大幅な効率化が期待されています:
- 候補化合物の探索:AI基盤モデルが膨大な化合物ライブラリから有望な候補を短時間で特定
- 薬物動態予測:体内での薬物の吸収、分布、代謝、排泄を高精度にシミュレーション
- 副作用予測:複雑な生物学的ネットワークを考慮し、潜在的な副作用を事前に予測
- 臨床試験デザイン最適化:最適な被験者選択と試験デザインによる成功率向上
これにより、開発期間の短縮、成功率の向上、コスト削減が実現し、より多くの革新的治療法が患者に届けられるようになるでしょう。
デジタルバイオロジーの現実的応用事例
理論だけでなく、すでに具体的な成果が出ている応用事例を見ていきましょう。
多がん早期検出技術
韓国MSITが発表した2025年の有望バイオテクノロジーの一つに「多がん早期検出」があります。従来のがん検査は単一のがん種に特化した手法が主流でしたが、AI基盤モデルを活用することで、血液中の微量な腫瘍由来DNAやタンパク質バイオマーカーを分析し、複数のがん種を同時に早期発見できる技術が開発されています。
これにより、早期発見・早期治療が可能となり、がん治療の成功率向上と医療コスト削減が期待されています。
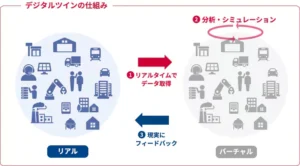
医療デジタルツイン
「医療デジタルツイン」も注目技術の一つです。これは患者個人の生理学的データ、遺伝情報、生活習慣などを統合したバーチャルな「分身」を作成し、様々な治療シナリオをシミュレーションする技術です。
- 治療効果予測:実際に薬剤を投与する前に、デジタルツインで効果を予測
- 手術シミュレーション:複雑な手術を事前にデジタル空間で試行
- 慢性疾患管理:長期的な健康状態の変化をシミュレーションし最適な治療法を探索
医療デジタルツインは、個別化医療の究極の形とも言えるでしょう。
バイオボットの開発
生体組織を用いた「バイオボット」も革新的な技術です。例えば、心筋細胞やニューロンなどの生きた細胞を組み込んだ微小ロボットは、体内での薬物送達や組織修復など、従来のロボット工学では実現できなかった機能を発揮します。
AI基盤モデルは、こうしたバイオボットの設計最適化や挙動予測に活用されており、再生医療や精密医療の新たな可能性を切り開いています。
課題と展望
革新的な技術にはチャレンジも伴います。デジタルバイオロジーとAI基盤モデルが直面する主な課題を整理しましょう。
現在の技術的課題
- データ品質と標準化:生物学データは多様かつ複雑で、標準化が難しい
- 説明可能性の確保:AIの判断プロセスが「ブラックボックス」化しやすい
- 計算リソースの制約:大規模なAI基盤モデルには膨大な計算リソースが必要
- 分野横断的な専門知識:AI・情報科学・生物学を横断する人材育成が急務
倫理的・社会的課題
- プライバシーとデータ保護:個人の遺伝情報などセンシティブデータの保護
- アクセスの公平性:革新的技術の恩恵が一部の富裕層だけに限定されるリスク
- バイアスと不平等:特定人種や集団のデータが少ない場合の予測精度格差
- 規制の適応:急速な技術革新に規制枠組みが追いつけない問題
将来展望
これらの課題を克服しながら、デジタルバイオロジーとAI基盤モデルは今後以下のような方向に発展していくでしょう:
- 生物学的アルゴリズムの発見:生命現象を制御する根本的な原理の解明
- シンセティック・バイオロジーの加速:人工的な生物システム設計の高度化
- 環境・気候問題への応用:微生物群集のモデリングによる環境浄化・修復
- 宇宙生物学との接点:地球外環境での生命探査・持続可能な居住環境の設計
専門家の見解
デジタルバイオロジーの分野で活躍する専門家たちは、この技術革新をどのように評価しているのでしょうか?
Latent LabsのCEOで創設者のSimon Kohlは次のように述べています:
「すべてのバイオテクノロジー企業や製薬企業は、最良の治療分子を見つけるためにテクノロジーの最先端にいたいと考えていますが、すべての企業がこの仕事に最先端のAIモデルを開発できる立場にあるわけではありません。そこでLatent Labsの出番です。私たちはジェネレーティブ・バイオロジー(生成生物学)の最前線を押し進め、パートナーに創薬プログラムを加速させるツールへの即時アクセスを提供します」
また、科学技術振興機構(JST)の報告によれば、「生命科学研究は従来の反復実験と観察から、予測と推論のための人工知能(AI)を組み込んだデータ駆動型アプローチへ移行している」と分析されています。
日本の研究動向と課題
世界的なデジタルバイオロジーの潮流の中で、日本の研究動向はどのようになっているでしょうか?
日本の現状
日本は基礎生物学研究では高い実績を持ちますが、バイオインフォマティクスやデジタルバイオロジーの分野では人材不足が課題となっています。バイオインフォマティクス人材は不足しており、市場拡大とともに人材不足はさらに深刻化すると予想されています。
また、計算機資源や研究予算の制約も大きな課題です。ただし、理化学研究所や産業技術総合研究所などの国立研究機関では、デジタルバイオロジーに関する先進的な研究プロジェクトが進行中です。
日本が優位性を発揮できる領域
日本が特に強みを発揮できる可能性があるのは以下の領域です:
- 高品質な臨床データ活用:国民皆保険制度の下での統一された医療データの活用
- 長寿研究への応用:世界一の長寿国としての高齢者データを活用した健康長寿研究
- 発酵・醸造技術との融合:伝統的な微生物活用技術とデジタルバイオロジーの融合
個人や中小企業にとっての意味
最後に、この技術革新が個人や中小企業にとってどのような意味を持つのかを考えてみましょう。
個人への影響
- 医療の個別化と高度化:自分に最適な予防・治療法へのアクセス向上
- 健康管理の変革:遺伝情報に基づくパーソナライズされた健康アドバイス
- 新しい職業機会:バイオインフォマティクスやAI生物学者など新しい職種の創出
中小企業や新興企業のチャンス
- 特化型AIサービス:特定の生物学的問題に特化したAIソリューション提供
- データ標準化・前処理:大規模研究機関や企業向けのデータ品質管理サービス
- 教育・トレーニング:専門家育成のためのプログラム提供
大手企業だけでなく、技術に精通した中小企業や個人起業家にも多くの機会が生まれるでしょう。
まとめ
デジタルバイオロジーとAI基盤モデルの融合は、これからの数年間でさらに加速することが予想されます。2025年の現時点では技術的・倫理的な課題も多いものの、医療、創薬、農業、環境科学など幅広い分野に革新をもたらす可能性を秘めています。
生物学のデジタル化は、単なる研究効率化だけでなく、生命現象の本質的な理解を深め、人類の健康と福祉に貢献する大きな可能性を持っています。今後、この分野の発展に注目し、適切な規制の下で技術革新の恩恵を社会全体で享受できる環境づくりが重要となるでしょう。
参考文献・引用元
- 「2025年の10大有望バイオテクノロジーを発表 韓国MSIT」 Science Portal
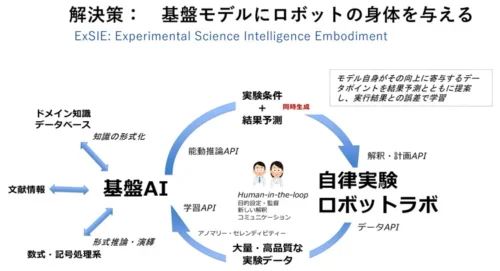
- 「AIにロボットの身体を与え、生命科学研究のラボを自律化する基盤」 Science Portal
- 「生物学をプログラム可能にするためのAI基盤モデルを構築しているLatent Labs」 CRISP Bio Blog
- 「医薬品・バイオテクノロジーにおける2025年の成長の機会トップ6」 GII
- 「バイオインフォマティクスの将来性」 アカリク
- 「原核単細胞生物のAIモデルEVOが全生物界のAIモデルEVO 2へと進化」 CRISP Bio Blog
画像引用元
- デジタルバイオロジーとAI:Science Portal
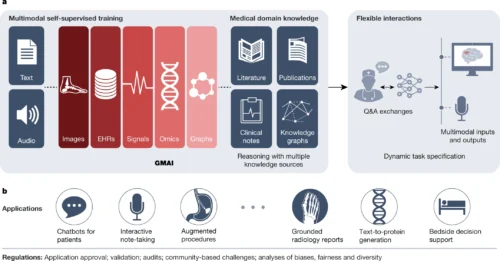
- バイオ基盤モデルのアーキテクチャ:Nature





コメント